Phương trình hóa học là một công cụ quan trọng trong việc mô tả các phản ứng hóa học giữa các chất. Tuy nhiên, để hiểu rõ hơn về bản chất của phản ứng và tính toán khối lượng hoặc thể tích của chất phản ứng và sản phẩm, việc cân bằng phương trình hóa học là điều cần thiết. Trong bài viết này, chúng ta sẽ tìm hiểu về tầm quan trọng của việc cân bằng phương trình hóa học và phương pháp cân bằng phương trình cho phản ứng Fe2O3 + HNO3 → Fe(NO3)3 + H2O.
Fe2O3 + HNO3 = Fe(NO3)3 + H2O
Đầu tiên, chúng ta hãy xem xét phản ứng hóa học giữa Fe2O3 và HNO3 để tạo thành Fe(NO3)3 và H2O. Phản ứng này có thể được biểu diễn dưới dạng phương trình hóa học như sau:
Fe2O3 + HNO3 → Fe(NO3)3 + H2O
Trong đó, Fe2O3 là công thức hóa học của sắt (III) oxit và HNO3 là công thức hóa học của axit nitric. Khi hai chất này phản ứng với nhau, ta thu được Fe(NO3)3 và H2O.
Tuy nhiên, để phản ứng diễn ra theo đúng tỷ lệ mol của chất phản ứng và sản phẩm, chúng ta cần cân bằng phương trình hóa học này. Điều này giúp chúng ta tính toán khối lượng hoặc thể tích của các chất cần thiết và các sản phẩm được tạo thành, từ đó dự đoán hiệu quả và khả năng tái sử dụng của các chất trong phản ứng.
Phương pháp cân bằng phương trình Fe2O3 + HNO3 → Fe(NO3)3 + H2O
Để cân bằng phương trình hóa học Fe2O3 + HNO3 → Fe(NO3)3 + H2O, chúng ta cần thực hiện các bước sau:
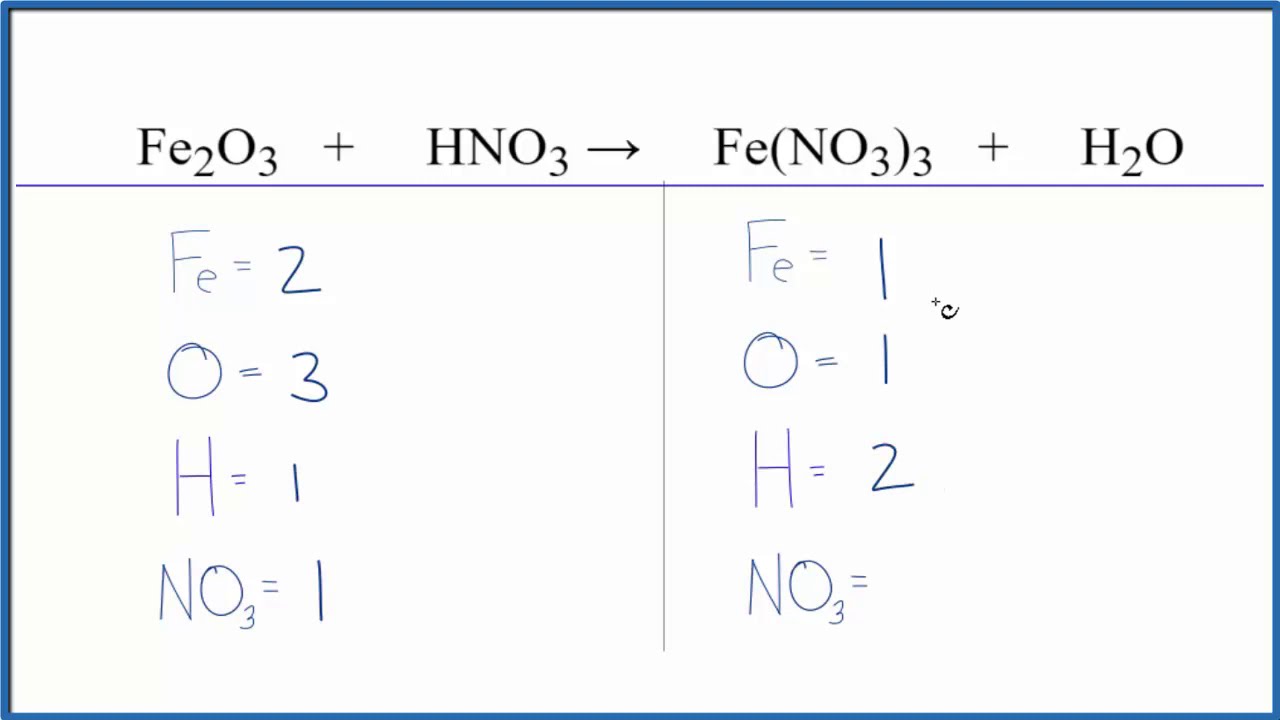
Bước 1: Xác định số nguyên tử của mỗi nguyên tố ở cả hai vế.
Trước khi bắt đầu cân bằng phương trình, chúng ta cần xác định số nguyên tử của mỗi nguyên tố ở cả hai vế của phương trình. Bảng dưới đây sẽ giúp chúng ta thấy rõ hơn số nguyên tử của mỗi nguyên tố trong phản ứng này:
| Yếu tố | Phía bên trái | Phía bên phải |
|---|---|---|
| Fe | 2 | 1 |
| Ồ | 3 | 9 |
| N | 0 | 3 |
| H | 0 | 3 |
Bước 2: Tìm hệ số cân bằng cho mỗi phần tử
Sau khi xác định số nguyên tử của mỗi nguyên tố ở cả hai vế, ta sẽ sử dụng hệ số n để cân bằng phương trình. Với phương trình Fe2O3 + HNO3 → Fe(NO3)3 + H2O, ta sẽ có:
2Fe2O3 + nHNO3 → 2Fe(NO3)3 + nH2O
Bước 3: Cân bằng từng yếu tố theo thứ tự
Tiếp theo, chúng ta sẽ cân bằng từng phần tử theo thứ tự từ trái sang phải và từ trên xuống dưới.
Cân bằng Fe
Đối với nguyên tố Fe, vế trái có 4 nguyên tử Fe, trong khi vế phải chỉ có 2 nguyên tử Fe. Để cân bằng số nguyên tử Fe ở cả hai vế, ta sẽ thêm hệ số 2 vào vế phải:
2Fe2O3 + nHNO3 → 4Fe(NO3)3 + nH2O
Số dư N
Đối với nguyên tố N, vế phải có 12 nguyên tử N. Để cân bằng số nguyên tử N ở cả hai vế, chúng ta sẽ thêm hệ số 6 vào vế trái:
6Fe2O3 + nHNO3 → 4Fe(NO3)3 + nH2O
Cân bằng H
Đối với nguyên tố H, vế phải có 12 nguyên tử H. Để cân bằng số nguyên tử H ở cả hai vế, ta sẽ thêm hệ số 6 vào vế trái:
6Fe2O3 + nHNO3 → 4Fe(NO3)3 + 6H2O
Cân bằng O
Cuối cùng, chúng ta sẽ cân bằng số nguyên tử O ở cả hai vế. Vế trái có 24 nguyên tử O, trong khi vế phải có 27 nguyên tử O. Chúng ta sẽ thêm hệ số 3 vào vế trái để cân bằng số nguyên tử O:
6Fe2O3 + nHNO3 → 4Fe(NO3)3 + 6H2O
Kết quả là chúng ta đã cân bằng được phương trình hóa học Fe2O3 + HNO3 → Fe(NO3)3 + H2O.
Fe2O3 + HNO3 = Fe(NO3)3 + NO + H2O
Tuy nhiên, trong một số trường hợp, việc cân bằng phương trình hóa học có thể không đơn giản như vậy. Ví dụ, nếu chúng ta muốn cân bằng phương trình Fe2O3 + HNO3 → Fe(NO3)3 + NO + H2O, chúng ta sẽ có:
2Fe2O3 + nHNO3 → 4Fe(NO3)3 + mNO + pH2O
Trong đó, m và p là hai hệ số cần tìm. Để cân bằng phương trình này, ta sẽ thực hiện các bước tương tự như trên và thu được kết quả sau:
6Fe2O3 + 5HNO3 → 4Fe(NO3)3 + 3NO + 9H2O
Fe2O3 + HNO3 = Fe(NO3)3 + NO2 + H2O
Một ví dụ khác, nếu chúng ta muốn cân bằng phương trình Fe2O3 + HNO3 → Fe(NO3)3 + NO2 + H2O, chúng ta sẽ có:
2Fe2O3 + nHNO3 → 4Fe(NO3)3 + mNO2 + pH2O
Thực hiện các bước tương tự như trên, ta sẽ có kết quả như sau:
6Fe2O3 + 5HNO3 → 4Fe(NO3)3 + 6NO2 + 9H2O
Fe2O3 + HNO3 = Fe(NO3)3 + H2O
Cuối cùng, nếu chúng ta muốn cân bằng phương trình Fe2O3 + HNO3 → Fe(NO3)3 + H2O, chúng ta sẽ có:
2Fe2O3 + nHNO3 → 4Fe(NO3)3 + pH2O
Thực hiện các bước tương tự như trên, ta sẽ có kết quả như sau:
6Fe2O3 + 5HNO3 → 4Fe(NO3)3 + 9H2O
Kết luận
Trong hóa học, cân bằng phương trình hóa học là yêu cầu thiết yếu để hiểu bản chất của phản ứng và tính toán khối lượng hoặc thể tích của chất phản ứng và sản phẩm. Trong bài viết này, chúng ta đã tìm hiểu về tầm quan trọng của việc cân bằng phương trình hóa học và phương pháp cân bằng phương trình cho phản ứng Fe2O3 + HNO3 → Fe(NO3)3 + H2O. Hy vọng bài viết này sẽ giúp bạn hiểu rõ hơn về quá trình cân bằng phương trình hóa học và áp dụng thành công vào các bài tập và thí nghiệm.
Mọi thắc mắc vui lòng gửi về Hotline 09633458xxx hoặc địa chỉ email [email protected] để làm rõ. Trân trọng!
Tuyên bố miễn trừ trách nhiệm: sesua.vn là website tổng hợp kiến thức từ nhiều nguồn,Vui lòng gửi email cho chúng tôi nếu có bất cứ vi phạm bản quyền nào! Xin cám ơn!














