Phản ứng hóa học là quá trình xảy ra khi hai hay nhiều chất tương tác với nhau, tạo ra sản phẩm mới có tính chất khác so với chất ban đầu. Trong đó, phản ứng giữa Ca(OH)2 và NaHCO3 là một trong những phản ứng hóa học quan trọng và được sử dụng rộng rãi trong thực tế. Trong bài viết này, chúng ta sẽ tìm hiểu về cơ chế, điều kiện và ứng dụng của phản ứng này.
Điều chế CaCO3 từ phản ứng của Ca(OH)2 và NaHCO3
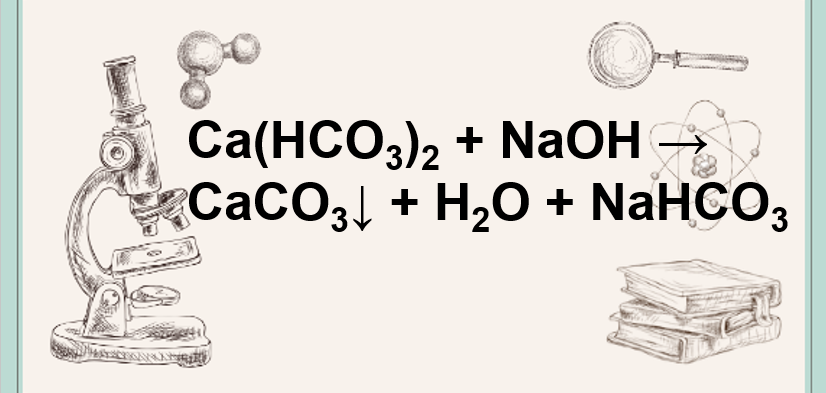
Phản ứng giữa Ca(OH)2 và NaHCO3 tạo ra CaCO3 (canxi cacbonat) là sản phẩm chính, cùng với H2O (nước) và NaOH (natri hydroxit). Đây là phản ứng trung hòa, nghĩa là sản phẩm cuối cùng có độ axit và độ kiềm bằng nhau.
Công thức phản ứng hóa học: Ca(OH)2 + NaHCO3 → CaCO3 ↓ + H2O + NaOH
Trong đó:
- Ca(OH)2 là canxi hiđroxit, một hợp chất vô cơ có tính bazơ mạnh.
- NaHCO3 là natri bicacbonat, còn được gọi là baking soda, là muối của axit cacbonic và natri, một bazơ nhẹ.
- CaCO3 là canxi cacbonat, một hợp chất vô cơ có tính bazơ vừa phải.
- H2O là nước, một hợp chất vô cơ không có tính bazơ cũng không có tính axit.
- NaOH là natri hiđroxit, một hợp chất vô cơ có tính bazơ mạnh.
Phản ứng giữa Ca(OH)2 và NaHCO3 xảy ra khi hai chất này tiếp xúc với nhau trong môi trường nước. Khi đó, các phân tử Ca(OH)2 sẽ tương tác với các phân tử nước, tạo thành các ion Ca2+ và ion OH-. Tương tự, các phân tử NaHCO3 cũng sẽ tương tác với nước, tạo thành các ion Na+ và ion HCO3-. Các ion này sẽ tương tác với nhau, tạo thành các sản phẩm cuối cùng là CaCO3, H2O và NaOH.
Cơ chế phản ứng giữa Ca(OH)2 và NaHCO3
Cơ chế phản ứng giữa Ca(OH)2 và NaHCO3 được giải thích bằng thuyết axit-bazơ. Theo đó, Ca(OH)2 là một bazơ mạnh, có khả năng nhận proton để tạo thành ion OH-. Trong khi đó, NaHCO3 là một bazơ yếu, có khả năng nhận proton để tạo thành ion HCO3-. Khi hai chất này tiếp xúc với nhau trong môi trường nước, các ion OH- và HCO3- sẽ tương tác với nhau, tạo thành sản phẩm cuối cùng là CaCO3, H2O và NaOH.
Ứng dụng của phản ứng Ca(OH)2 và NaHCO3 trong thực tế

Phản ứng giữa Ca(OH)2 và NaHCO3 có nhiều ứng dụng thực tế, từ công nghiệp đến dân dụng. Dưới đây là một số ứng dụng phổ biến của phản ứng này:
Sản xuất canxi cacbonat
Sản phẩm chính của phản ứng giữa Ca(OH)2 và NaHCO3 là canxi cacbonat, có nhiều tính chất hữu ích. Do đó, phản ứng này được sử dụng để sản xuất canxi cacbonat trên quy mô lớn trong công nghiệp. Canxi cacbonat được sử dụng trong sản xuất giấy, nhựa, sơn, thuốc trừ sâu và nhiều sản phẩm khác.
Tăng độ cứng của nước
Nước có tính axit thấp (pH
Được sử dụng trong sản xuất bột giặt
Bột giặt là một trong những sản phẩm không thể thiếu trong cuộc sống hiện đại. Để tạo ra bột giặt, người ta thường sử dụng phản ứng giữa Ca(OH)2 và NaHCO3. Khi hai chất này tiếp xúc với nhau trong môi trường nước sẽ tạo ra canxi cacbonat, làm cho bột giặt có tính kiềm, giúp loại bỏ vết bẩn và bảo vệ da tay khi sử dụng.
Cơ chế phản ứng giữa Ca(OH)2 và NaHCO3

Cơ chế phản ứng giữa Ca(OH)2 và NaHCO3 được giải thích bằng thuyết axit-bazơ. Theo đó, Ca(OH)2 là một bazơ mạnh, có khả năng nhận proton để tạo thành ion OH-. Trong khi đó, NaHCO3 là một bazơ yếu, có khả năng nhận proton để tạo thành ion HCO3-. Khi hai chất này tiếp xúc với nhau trong môi trường nước, các ion OH- và HCO3- sẽ tương tác với nhau, tạo thành sản phẩm cuối cùng là CaCO3, H2O và NaOH.
Điều kiện phản ứng của Ca(OH)2 với NaHCO3
Để phản ứng giữa Ca(OH)2 và NaHCO3 xảy ra, cần có một số điều kiện sau:
- Môi trường nước: Phản ứng chỉ xảy ra khi hai chất tiếp xúc với nhau trong môi trường nước.
- Nhiệt độ: Nhiệt độ cũng ảnh hưởng đến tốc độ và hiệu quả của phản ứng. Nhìn chung, nhiệt độ cao sẽ làm tăng tốc độ phản ứng, nhưng nhiệt độ quá cao cũng có thể làm giảm hiệu quả của phản ứng.
- Nồng độ: Nồng độ của các chất trong phản ứng cũng ảnh hưởng đến tốc độ và hiệu quả của phản ứng. Nhìn chung, khi nồng độ của một chất tăng, tốc độ phản ứng cũng sẽ tăng.
Vai trò của Ca(OH)2 và NaHCO3 trong phản ứng
Trong phản ứng giữa Ca(OH)2 và NaHCO3, hai chất này đều đóng vai trò quan trọng và không thể thiếu. Cụ thể:
- Ca(OH)2: Là chất khởi đầu phản ứng, có tính bazơ mạnh và có khả năng nhận proton để tạo thành ion OH-. Đây là chất đóng vai trò quyết định trong phản ứng.
- NaHCO3: Là một bazơ nhẹ, có khả năng nhận proton để tạo thành ion HCO3-. Chất này cũng đóng vai trò quan trọng trong việc tạo ra các sản phẩm cuối cùng là CaCO3, H2O và NaOH.
Sản phẩm hình thành từ phản ứng của Ca(OH)2 và NaHCO3
Phản ứng giữa Ca(OH)2 và NaHCO3 tạo ra ba sản phẩm chính: CaCO3, H2O và NaOH. Các sản phẩm này có tính chất khác nhau và được sử dụng trong nhiều lĩnh vực khác nhau.
CaCO3 (canxi cacbonat)
Canxi cacbonat là sản phẩm chính của phản ứng giữa Ca(OH)2 và NaHCO3. Đây là hợp chất vô cơ có độ bazơ trung bình, được sử dụng rộng rãi trong công nghiệp và dân dụng. Canxi cacbonat có màu trắng, không tan trong nước và có độ cứng cao, là nguyên liệu quan trọng trong sản xuất giấy, nhựa, sơn và nhiều sản phẩm khác.
H2O (nước)
Nước là sản phẩm không thể thiếu trong phản ứng giữa Ca(OH)2 và NaHCO3. Nước không có tính axit cũng không có tính bazơ, là hợp chất vô cơ không thể thiếu trong cuộc sống của con người. Nước được sử dụng trong nhiều lĩnh vực, từ sản xuất đến sinh hoạt hàng ngày.
NaOH (natri hiđroxit)
Natri hiđroxit là sản phẩm cuối cùng của phản ứng giữa Ca(OH)2 và NaHCO3. Đây là một bazơ vô cơ mạnh và được sử dụng trong nhiều lĩnh vực khác nhau. Natri hiđroxit có tính ăn mòn và nên thận trọng khi sử dụng trong công nghiệp và gia dụng.
Ảnh hưởng của nồng độ đến phản ứng của Ca(OH)2 với NaHCO3
Nồng độ của các chất trong phản ứng ảnh hưởng đến tốc độ và hiệu suất của phản ứng. Trong trường hợp phản ứng giữa Ca(OH)2 và NaHCO3, nồng độ của hai chất này cũng đóng vai trò quan trọng.
Khi nồng độ Ca(OH)2 tăng, tốc độ phản ứng cũng sẽ tăng. Điều này là do khi nồng độ Ca(OH)2 tăng, số phân tử Ca(OH)2 có khả năng phản ứng với nước cũng tăng, do đó làm tăng tốc độ phản ứng.
Tương tự như vậy, khi nồng độ NaHCO3 tăng, tốc độ phản ứng cũng sẽ tăng. Điều này là do khi nồng độ NaHCO3 tăng, số lượng phân tử NaHCO3 có thể phản ứng với nước cũng tăng, do đó làm tăng tốc độ phản ứng.
Ảnh hưởng của nhiệt độ đến phản ứng của Ca(OH)2 và NaHCO3
Nhiệt độ cũng ảnh hưởng đến tốc độ và hiệu suất phản ứng giữa Ca(OH)2 và NaHCO3. Nhìn chung, nhiệt độ càng cao thì tốc độ phản ứng càng nhanh. Tuy nhiên, quá nhiệt cũng có thể làm giảm hiệu suất phản ứng.
Khi nhiệt độ tăng, động năng của các phân tử trong hệ thống cũng tăng, do đó làm tăng khả năng va chạm giữa các phân tử và tăng tốc độ phản ứng. Tuy nhiên, quá nhiệt cũng có thể làm giảm hiệu quả của phản ứng vì các phân tử có thể bị phá hủy hoặc chuyển đổi thành các chất khác.
Tóm tắt phản ứng hóa học giữa Ca(OH)2 và NaHCO3
Phản ứng giữa Ca(OH)2 và NaHCO3 là một trong những phản ứng hóa học quan trọng và được sử dụng rộng rãi trong thực tế. Hai chất này đóng vai trò quan trọng và không thể thiếu trong phản ứng, tạo ra ba sản phẩm chính: CaCO3, H2O và NaOH. Nồng độ và nhiệt độ cũng ảnh hưởng đến tốc độ và hiệu suất của phản ứng này.
Kết luận
Phản ứng giữa Ca(OH)2 và NaHCO3 là phản ứng hóa học quan trọng và được sử dụng rộng rãi trong thực tế. Đây là phản ứng đơn giản nhưng có tính ứng dụng cao, tạo ra các sản phẩm có tính chất khác nhau và được sử dụng trong nhiều lĩnh vực khác nhau. Nồng độ và nhiệt độ cũng ảnh hưởng đến tốc độ và hiệu suất của phản ứng này, vì vậy cần phải kiểm soát cẩn thận trong quá trình sử dụng.
Mọi thắc mắc vui lòng gửi về Hotline 09633458xxx hoặc địa chỉ email [email protected] để làm rõ. Trân trọng!
Tuyên bố miễn trừ trách nhiệm: sesua.vn là website tổng hợp kiến thức từ nhiều nguồn,Vui lòng gửi email cho chúng tôi nếu có bất cứ vi phạm bản quyền nào! Xin cám ơn!
- Cách pha mắm tôm ăn bún đậu ngon chuẩn vị đậm đà khó quên
- Cap đi biển, Status đi biển, STT đi biển hay thả thính dạo đỉnh cao
- Hướng Dẫn Cách Đóng Dấu Treo, Cách Đóng Dấu Giáp Lai 2023: Đảm Bảo Tính Pháp Lý Cho Văn Bản
- Cách bảo quản bưởi chín giữ được ngon múi tươi lâu
- Cách bảo quản dâu tây được lâu mà vẫn tươi ngon đơn giản














