Dãy điện hóa của kim loại là một khái niệm quan trọng trong lĩnh vực hóa học. Nó giúp chúng ta hiểu được tính chất và hành vi của kim loại trong các phản ứng hóa học. Trong bài viết này, chúng ta sẽ tìm hiểu về dãy điện hóa của kim loại, nguyên lý hoạt động, ứng dụng và vai trò của nó trong hóa học.
Khái niệm dãy điện hóa của kim loại
Dãy điện hóa của kim loại là bảng xếp hạng các kim loại dựa trên tính chất điện hóa của chúng. Nó cho biết vị trí của mỗi kim loại trong các phản ứng oxy hóa và khử. Các kim loại được sắp xếp theo thứ tự từ kim loại khử mạnh nhất đến kim loại oxy hóa mạnh nhất.
Đây là công cụ hữu ích để dự đoán tính chất hóa học của kim loại trong các phản ứng. Ngoài ra, dãy điện hóa của kim loại cũng giúp chúng ta hiểu được các quá trình điện hóa và cân bằng điện hóa trong các phản ứng.
Nguyên lý dãy điện hóa của kim loại
Nguyên lý của dãy điện hóa kim loại được nhà hóa học người Đức Johann Wolfgang Döbereiner đề xuất vào năm 1829. Ông nhận thấy có mối tương quan giữa tính khử và tính oxi hóa của kim loại. Kim loại có tính khử mạnh sẽ có tính oxi hóa yếu và ngược lại.
Sau đó, nhà hóa học người Anh Humphry Davy đã tiến hành nghiên cứu về tính chất điện hóa của kim loại và đưa ra dãy điện hóa kim loại hiện đại như chúng ta biết ngày nay.
Ứng dụng của dãy điện hóa của kim loại
Dãy điện hóa của kim loại có nhiều ứng dụng trong đời sống và trong lĩnh vực khoa học. Một trong những ứng dụng quan trọng nhất của dãy điện hóa là trong công nghệ điện hóa.
Các quá trình điện hóa như mạ điện, mạ bạc, mạ vàng… đều dựa trên nguyên lý dãy điện hóa của kim loại. Nó cho phép chúng ta xác định kim loại nào có tính khử mạnh hơn và sẽ được sử dụng làm điện cực trong quá trình điện phân.
Ngoài ra, dãy điện hóa kim loại còn được sử dụng trong các ứng dụng y tế như trong chẩn đoán và điều trị bệnh. Các thiết bị y tế như máy đo đường huyết, máy xét nghiệm máu… đều sử dụng nguyên lý dãy điện hóa kim loại để hoạt động.
Vị trí của kim loại trong dãy điện hóa
Trong dãy điện hóa kim loại, các kim loại được sắp xếp theo thứ tự từ chất khử mạnh nhất đến chất oxi hóa mạnh nhất. Kim loại có chất khử mạnh nhất là Liti (Li), kim loại có chất oxi hóa mạnh nhất là Flo (F).
Bảng dưới đây cho biết vị trí của kim loại trong dãy điện hóa của kim loại:
| STT | Tên | Biểu tượng | Vị trí trong dãy điện hóa |
|---|---|---|---|
| 1 | Liti | Lý | Chất khử mạnh nhất |
| 2 | Kali | K | |
| 3 | canxi | Bài hát | |
| 4 | Natri | Na | |
| 5 | Magiê | Mg | |
| 6 | Nhôm | Al | |
| 7 | Kẽm | Kẽm | |
| 8 | Sắt | Fe | |
| 9 | Tin tưởng | Sn | |
| 10 | Chỉ huy | Chì | |
| 11 | Hiđrô | H | |
| 12 | Đồng | Cu | |
| 13 | Bạc | Nông nghiệp | |
| 14 | Vàng | Âu | |
| 15 | Bạch kim | Phần | |
| 16 | Thủy ngân | Hg | |
| 17 | Flo | F | Chất oxy hóa mạnh nhất |
Chuỗi hoạt động của kim loại
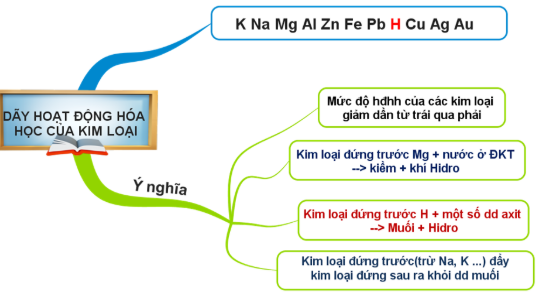
Dãy hoạt động của kim loại là một khái niệm liên quan đến dãy điện hóa của kim loại. Nó thể hiện tính khử và tính oxi hóa của các ion kim loại trong dung dịch.
Các ion kim loại có thể được chuyển đổi thành các nguyên tố tương ứng của chúng thông qua phản ứng oxy hóa khử. Vị trí của các ion kim loại trong chuỗi hoạt động xác định khả năng tham gia của chúng vào các phản ứng này.
Ví dụ, trong dung dịch axit clohydric (HCl), ion sắt (Fe) sẽ bị oxy hóa thành ion sắt (Fe3+) và ion hydro sẽ bị khử thành nguyên tố hydro. Tuy nhiên, trong dung dịch axit nitric (HNO3), ion sắt (Fe) sẽ không bị oxy hóa do vị trí của nó trong chuỗi hoạt động hóa học.
Ảnh hưởng của nồng độ ion kim loại đến vị trí trong dãy điện hóa
Ngoài tính chất điện hóa của kim loại, nồng độ ion kim loại cũng ảnh hưởng đến vị trí của chúng trong dãy điện hóa. Khi nồng độ ion kim loại tăng, tính khử của chúng giảm và tính oxi hóa của chúng tăng.
Điều này có thể được giải thích bởi thực tế là các ion kim loại có xu hướng kết hợp với nhau để tạo thành phức chất. Các phức chất này có tính oxy hóa mạnh hơn ion kim loại ban đầu, do đó khi nồng độ ion kim loại tăng, tính chất oxy hóa của chúng cũng tăng theo.
Ví dụ, trong dung dịch axit clohydric (HCl), nồng độ ion sắt (Fe) càng cao thì tính chất oxy hóa của nó càng tăng. Tuy nhiên, trong dung dịch axit nitric (HNO3), nồng độ ion sắt (Fe) không ảnh hưởng đến tính chất oxy hóa của nó do vị trí của nó trong chuỗi hoạt động hóa học.
Tầm quan trọng của dãy điện hóa của kim loại
Dãy điện hóa của kim loại là một khái niệm rất quan trọng trong hóa học. Nó giúp chúng ta hiểu được tính chất và hành vi của kim loại trong các phản ứng hóa học. Ngoài ra, nó còn có những ứng dụng quan trọng trong cuộc sống và trong lĩnh vực khoa học.
Trong công nghệ điện hóa, dãy điện hóa của kim loại giúp chúng ta dự đoán tính chất của kim loại trong quá trình điện phân và lựa chọn điện cực phù hợp. Điều này giúp tiết kiệm chi phí và tăng hiệu quả trong sản xuất.
Ngoài ra, dãy điện hóa kim loại cũng đóng vai trò quan trọng trong y học. Các thiết bị y tế như máy đo đường huyết, máy xét nghiệm máu, v.v. đều sử dụng nguyên lý dãy điện hóa kim loại để hoạt động. Điều này giúp chẩn đoán và điều trị bệnh hiệu quả hơn.
Cân bằng điện hóa và dãy điện hóa của kim loại
Cân bằng điện hóa là một quá trình quan trọng trong hóa học cho phép duy trì sự cân bằng các ion trong dung dịch. Trong quá trình này, các ion di chuyển từ điện cực dương sang điện cực âm và ngược lại.
Dãy điện hóa của kim loại đóng vai trò quan trọng trong cân bằng điện hóa. Nó chỉ ra tính chất điện hóa của kim loại và giúp dự đoán chuyển động của các ion trong quá trình cân bằng điện hóa.
Ví dụ, trong quá trình điện phân dung dịch natri clorua (NaCl), các ion natri (Na+) sẽ di chuyển từ điện cực âm sang điện cực dương và các ion clo (Cl-) sẽ di chuyển từ điện cực dương sang điện cực âm. Điều này được giải thích bằng vị trí của natri và clo trong dãy điện hóa của kim loại.
Sơ đồ dãy điện hóa của kim loại
Sơ đồ dãy điện hóa của kim loại là sơ đồ thể hiện vị trí của các kim loại trong dãy điện hóa, giúp ta dễ dàng nhận biết tính khử, tính oxi hóa của từng kim loại và mối tương quan giữa chúng.
Dưới đây là sơ đồ dãy điện hóa của kim loại:
Từ sơ đồ này, ta thấy các kim loại có tính khử mạnh nhất nằm ở phía bên trái và các kim loại có tính oxi hóa mạnh nhất nằm ở phía bên phải. Các kim loại ở giữa có tính khử và tính oxi hóa cân bằng.
Vai trò của dãy điện hóa của kim loại trong hóa học
Dãy điện hóa của kim loại đóng vai trò quan trọng trong hóa học. Nó giúp chúng ta hiểu được tính chất và hành vi của kim loại trong các phản ứng hóa học. Ngoài ra, nó còn có những ứng dụng quan trọng trong cuộc sống và trong lĩnh vực khoa học.
Trong công nghệ điện hóa, dãy điện hóa của kim loại giúp chúng ta dự đoán tính chất của kim loại trong quá trình điện phân và lựa chọn điện cực phù hợp. Điều này giúp tiết kiệm chi phí và tăng hiệu quả trong sản xuất.
Ngoài ra, dãy điện hóa kim loại cũng đóng vai trò quan trọng trong y học. Các thiết bị y tế như máy đo đường huyết, máy xét nghiệm máu, v.v. đều sử dụng nguyên lý dãy điện hóa kim loại để hoạt động. Điều này giúp chẩn đoán và điều trị bệnh hiệu quả hơn.
Kết luận
Dãy điện hóa của kim loại là một khái niệm quan trọng trong hóa học. Nó cho biết vị trí của kim loại trong các phản ứng oxy hóa và khử và có nhiều ứng dụng trong đời sống và khoa học.
Chúng ta đã tìm hiểu về khái niệm dãy điện hóa của kim loại, nguyên lý hoạt động, ứng dụng và vai trò của nó trong hóa học. Ngoài ra, chúng ta cũng tìm hiểu về vị trí của kim loại trong dãy điện hóa, dãy hoạt động hóa học của kim loại và ảnh hưởng của nồng độ ion kim loại đến vị trí trong dãy điện hóa.
Dãy điện hóa của kim loại đóng vai trò quan trọng trong việc giải thích các phản ứng hóa học và trong các ứng dụng công nghệ và y học. Hiểu rõ về dãy điện hóa của kim loại sẽ giúp chúng ta ứng dụng hiệu quả trong cuộc sống và trong lĩnh vực khoa học.
Mọi thắc mắc vui lòng gửi về Hotline 09633458xxx hoặc địa chỉ email [email protected] để làm rõ. Trân trọng!
Tuyên bố miễn trừ trách nhiệm: sesua.vn là website tổng hợp kiến thức từ nhiều nguồn,Vui lòng gửi email cho chúng tôi nếu có bất cứ vi phạm bản quyền nào! Xin cám ơn!














