Axit axetic (CH3COOH) là một trong những axit yếu phổ biến nhất trong cuộc sống hàng ngày. Nó được sử dụng trong nhiều lĩnh vực khác nhau như công nghiệp, y học và gia dụng. Trong bài viết này, chúng ta sẽ tìm hiểu về các tính chất của axit axetic và cách nó tương tác với các chất khác, đặc biệt là với natri cacbonat và natri axetat.
Natri cacbonat và natri axetat

Natri cacbonat (Na2CO3) và natri axetat (CH3COONa) là hai bazơ yếu. Chúng thường được dùng để trung hòa axit trong các phản ứng hóa học. Trước khi đi sâu vào chi tiết về phản ứng trung hòa giữa axit axetic và hai chất này, chúng ta cần hiểu tính chất của chúng.
Tính chất của natri cacbonat và natri axetat
Natri cacbonat là muối của axit cacbonic (H2CO3). Nó là bột màu trắng và hoàn toàn tan trong nước. Khi hòa tan trong nước, natri cacbonat tạo thành hai ion natri (Na+) và một ion cacbonat (CO32-). Điều này làm cho dung dịch natri cacbonat có tính bazơ, nghĩa là nó phản ứng với axit để tạo thành muối và nước.
Natri axetat cũng là muối của axit axetic. Nó là bột màu trắng và hoàn toàn tan trong nước. Khi hòa tan trong nước, natri axetat tạo thành hai ion natri (Na+) và một ion axetat (CH3COO-). Tương tự như natri cacbonat, dung dịch natri axetat cũng là một bazơ yếu.
Phản ứng trung hòa giữa axit axetic và natri cacbonat
 to a beaker containing 05 M hydrochloric acid In the reaction, HCl K2CO3 -- K.jpg)
Khi axit axetic tác dụng với natri cacbonat, phản ứng trung hòa sẽ xảy ra theo công thức sau:
CH3COOH + Na2CO3 → CH3COONa + H2O + CO2
Trong đó, CH3COOH là axit axetic, Na2CO3 là natri cacbonat, CH3COONa là natri axetat, H2O là nước và CO2 là cacbon dioxit.
Cơ chế phản ứng
Phản ứng trung hòa giữa axit axetic và natri cacbonat xảy ra theo cơ chế trao đổi ion. Ban đầu, các phân tử axit axetic sẽ tương tác với các ion natri trong dung dịch natri cacbonat để tạo thành muối natri axetat và giải phóng các ion hydro. Đồng thời, các ion cacbonat cũng sẽ tương tác với các ion hydro để tạo thành nước và giải phóng CO2. Kết quả là, chúng ta thu được dung dịch chứa muối natri axetat, nước và khí CO2.
Thay đổi độ pH
Trong phản ứng trung hòa giữa axit axetic và natri cacbonat, độ pH của dung dịch sẽ thay đổi. Ban đầu, dung dịch có tính axit do sự có mặt của axit axetic. Tuy nhiên, khi phản ứng diễn ra, các ion natri và cacbonat sẽ tương tác với nhau để tạo thành muối và nước, làm cho độ pH của dung dịch tăng lên. Điều này cho thấy natri cacbonat là một bazơ yếu và có khả năng trung hòa axit.
Phản ứng trung hòa giữa axit axetic và natri axetat
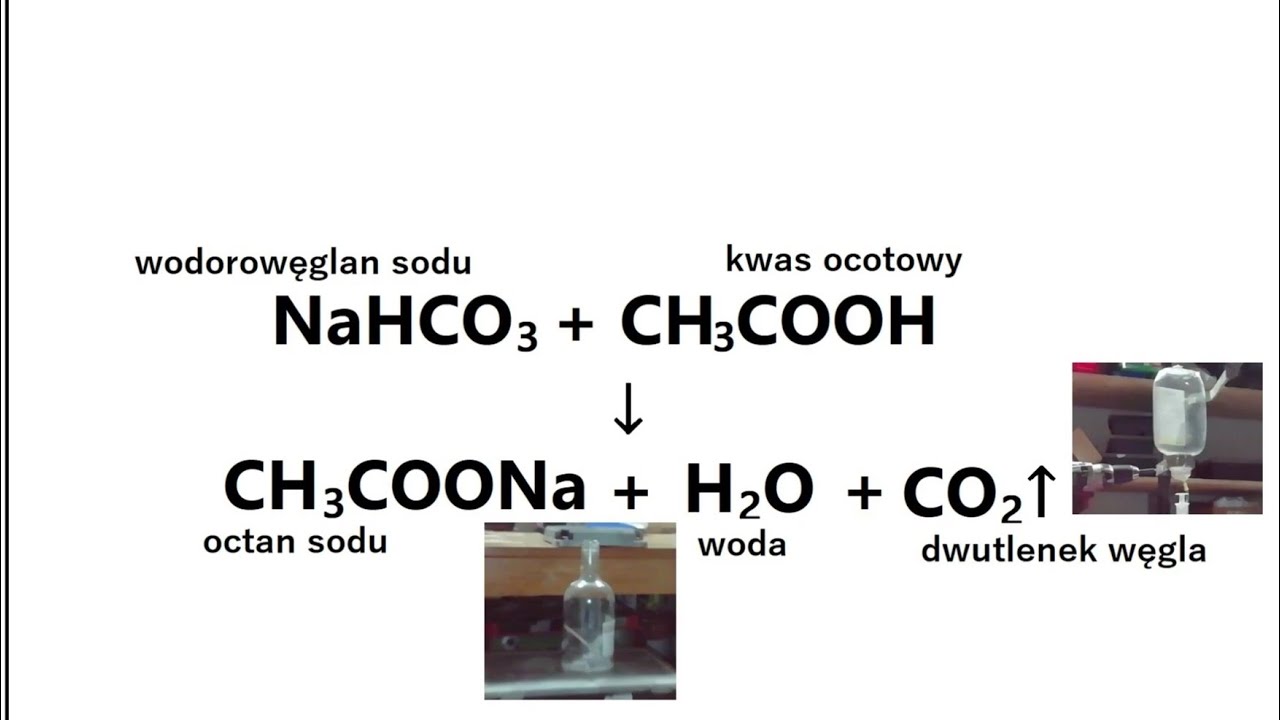
Phản ứng trung hòa giữa axit axetic và natri axetat cũng diễn ra theo cơ chế trao đổi ion, tương tự như phản ứng giữa axit axetic và natri cacbonat. Công thức phản ứng là:
CH3COOH + CH3COONa → CH3COONa + H2O
Trong đó, CH3COOH là axit axetic, CH3COONa là natri axetat, CH3COONa là muối natri axetat và H2O là nước.
Thay đổi độ pH
Tương tự như phản ứng giữa axit axetic và natri cacbonat, khi tương tác với natri axetat, độ pH của dung dịch cũng sẽ tăng do tính bazơ yếu của natri axetat. Điều này chứng tỏ natri axetat cũng có khả năng trung hòa axit.
Dung dịch axit yếu và bazơ yếu
Axit axetic và natri cacbonat đều là axit yếu và bazơ yếu. Vậy điều gì khiến chúng có những tính chất này?
Axit yếu
Axit yếu là những chất có khả năng tạo ra ít ion hydro trong dung dịch. Điều này làm cho dung dịch có nồng độ ion H+ thấp, tạo thành axit yếu. Trong trường hợp axit axetic, khi hòa tan trong nước, chỉ một phần nhỏ các phân tử axit sẽ tạo thành ion H+, phần còn lại sẽ tồn tại dưới dạng các phân tử không phản ứng. Điều này làm cho axit axetic trở thành axit yếu.
Cơ sở yếu
Bazơ yếu là những chất tạo ra ít ion hydroxyl (OH-) trong dung dịch. Tương tự như axit axetic, khi hòa tan trong nước, chỉ một phần nhỏ natri cacbonat và natri axetat sẽ tạo thành ion OH-, phần còn lại sẽ tồn tại dưới dạng các phân tử không phản ứng. Điều này làm cho natri cacbonat và natri axetat trở thành bazơ yếu.
Chất điện phân và tính chất của chúng
Chất điện giải là những chất có khả năng tạo ra ion khi hòa tan trong nước. Trong trường hợp axit axetic, natri cacbonat và natri axetat, khi hòa tan trong nước, tất cả chúng đều tạo ra ion để tạo thành dung dịch. Điều này làm cho chúng trở thành chất điện giải.
Tính chất điện của một chất được đo bằng độ dẫn điện của dung dịch chứa nó. Chất điện phân mạnh có độ dẫn điện cao, trong khi chất điện phân yếu có độ dẫn điện thấp. Trong trường hợp axit axetic, natri cacbonat và natri axetat, tất cả chúng đều có độ dẫn điện thấp do tính chất yếu của chúng.
Kết luận
Trong bài viết này, chúng ta đã tìm hiểu về tính chất của axit axetic và cách nó tương tác với các chất khác như natri cacbonat và natri axetat. Chúng ta đã thấy rằng phản ứng trung hòa giữa axit axetic và hai chất này diễn ra theo cơ chế trao đổi ion và tạo ra muối và nước. Chúng ta cũng đã tìm hiểu về tính chất của axit yếu và bazơ yếu, cũng như tính chất điện phân của các chất này. Hy vọng rằng bài viết này sẽ giúp bạn hiểu rõ hơn về axit axetic và phản ứng trung hòa trong hóa học.
Mọi thắc mắc vui lòng gửi về Hotline 09633458xxx hoặc địa chỉ email [email protected] để làm rõ. Trân trọng!
Tuyên bố miễn trừ trách nhiệm: sesua.vn là website tổng hợp kiến thức từ nhiều nguồn,Vui lòng gửi email cho chúng tôi nếu có bất cứ vi phạm bản quyền nào! Xin cám ơn!














